Comments
Synonyme: Sachharose, Sucrose, α-D-Glucopyranosyl-(1-2)-β-D-fructofuranosid, β-D-Fructofuranosyl-α-D-glucopyranosid, Kristallzucker, Rohrzucker, Rübenzucker, Haushaltszucker, SUCROSE (INCI)
Über Saccharose
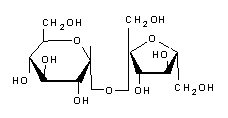
Saccharose oder Saccarose ist ein Zucker mit einem süßen Geschmack. Sie wird aus bestimmten Pflanzen, vor allem aus Zuckerrohr und Zuckerrüben, gewonnen und in der menschlichen Ernährung sehr häufig verwendet. Es handelt sich um ein aus Glucose und Fructose bestehendes Diholosid, dessen normalisierte Bezeichnung α-D-Glucopyranosyl-(1↔2)-β-D-fructofuranosid lautet, üblicherweise abgekürzt als Glc-Fru. Im Englischen wird es als Sucrose bezeichnet, daher die in der Literatur manchmal anzutreffende Abkürzung Suc für diese Verbindung. - Kohlenhydrate, insbesondere Saccharose, wurden früher aufgrund eines alten Experiments zur Dehydrierung von weißem Zucker mit konzentrierter Schwefelsäure als Kohlenhydrate bezeichnet, bei dem die Saccharose mit der Summenformel C12H22O11 in Wasser H2O und Ruß zerlegt wurde. Daraus hatte man fälschlicherweise abgeleitet, dass die Formel für Saccharose (H2O)11C12 geschrieben werden könnte, was einem Kohlenhydrat entspräche. Die Bezeichnung wurde durch die Arbeiten von Walter Norman Haworth, der Anfang des 20. Jahrhunderts die Struktur der Kohlenhydrate festlegte, überholt und ist seitdem nicht mehr gebräuchlich. In der englischsprachigen Welt ist der Begriff jedoch nach wie vor gebräuchlich. – Eigenschaften – Struktur - Das Saccharosemolekül ist ein Diholosid, das aus einem Glucoserest und einem Fructoserest besteht, die durch eine osidische Bindung α(1↔2)β verbunden sind. Seine Summenformel lautet C12H22O11 und seine molare Masse beträgt 342,3 g mol-1. Im Gegensatz zu den meisten anderen Diholosiden entsteht Saccharose durch die Verknüpfung zweier Osen an ihren reduzierenden Enden, was sie zu einem nichtreduzierenden Zucker macht. Außerdem bilden nur das α-Anomer von Glucopyranose und das β-Anomer von Fructofuranose die Saccharose. - Die Saccharose kristallisiert im monoklinen Kristallsystem gemäß der Raumgruppe P21 mit den Kristallparametern a = 1,086 31 nm, b = 0,870 44 nm, c = 0,776 24 nm und β = 102,938° - Die Reinheit der Saccharose wird polarimetrisch gemessen. Genauer gesagt wird die Drehung der Polarisationsebene von polarisiertem Licht gemessen, das durch eine wässrige Zuckerlösung fällt. Die spezifische Drehung (en) bei 20 °C, gemessen mithilfe der Natrium-D-Linie bei 589 nm, beträgt +66,47°. Kommerzielle Saccharose wird auf diese Weise kontrolliert. Unter normalen Bedingungen verschlechtert sie sich nicht. - Saccharose hat fünf natürliche Isomere, die sich in der Position der osidischen Bindung unterscheiden: Trehalulose ⇒ Glucose α(1→1) Fructose; Turanose ⇒ Glucose α(1→3) Fructose (reduzierendes Diholosid) ; Maltulose ⇒ Glucose α(1→4) Fructose ; Leucrose ⇒ Glucose α(1→5) Fructose (reduzierendes Diholosid) ; Isomaltulose (Palatinose) ⇒ Glucose α(1→6) Fructose (reduzierendes Diholosid). - Reaktionen mit Saccharose - Verschiedene chemische Umwandlungen mit Saccharose als Reaktant sind denkbar: - Thermische Zersetzung - Die thermische Zersetzung von Saccharose kann als eine zweistufige Reaktion dargestellt werden: -zunächst eine Dehydratisierung (durch Schwefelsäure H2SO4), bei der Wasser und Ruß entstehen: - C12H22O11 → 12 C + 11 H2O ; - und dann die Oxidation (mit dem Sauerstoff der Luft) von Kohlenstoff zu Kohlendioxid : - 12 C + 12 O2 → 12 CO2. – Karamellisierung - Saccharose schmilzt nicht, wenn sie erhitzt wird, sondern zersetzt sich bei etwa 186 °C zu Karamell. – Verbrennung - Saccharose verbrennt in einer exothermen Reaktion unter Bildung von Wasser und Kohlendioxid, wie es alle Kohlenhydrate tun. - Mit Chlorsäure - Mit der Chlorsäure HClO3 setzt Saccharose Wasser, Kohlendioxid und Chlorwasserstoff (HCl) frei : - 8 HClO3 + C12H22O11 → 11 H2O + 12 CO2 + 8 HCl. - Chemische Eigenschaften - Saccharose ist ein nichtreduzierender Zucker , der Hemiacetalkohlenstoff der Glucose und der Hemiacetalkohlenstoff der Fructose sind an der osidischen Bindung beteiligt. Sie ist nicht hygroskopisch und kann keine Mutarotation durchführen. – Hydrolyse - Die Hydrolyse von Saccharose bewirkt, dass die osidische Bindung gespalten wird, indem Glucose und Fructose in äquimolaren Mengen freigesetzt werden. Diese Reaktion ist jedoch so langsam, dass eine wässrige Saccharoselösung jahrelang praktisch stabil bleiben kann. In Gegenwart einer Saccharase (Saccharase-Isomaltase, Invertase, Saccharose-Alpha-Glucosidase) oder einer Säure wie Kaliumbitartrat HOOC-CHOH-CHOH-COOK oder Zitronensaft, die schwache Säuren sind, verläuft sie dagegen viel schneller. Dasselbe geschieht im Magensaft, der an der Verdauung beteiligt ist, indem er Kohlenhydrate wie Saccharose hydrolysiert. - Durch die Einwirkung von Invertase auf Saccharose entsteht Invertzucker, der aus gleichen Mengen Glukose und Fruktose besteht. - Biosynthese von Saccharose - Die Biosynthese von Saccharose wird von der Saccharose-Phosphat-Synthase aus UDP-Glucose und Fructose-6-Phosphat durchgeführt. Die für diese Reaktion benötigte Energie stammt aus der Spaltung von UDP. Saccharose wird von Pflanzen und Cyanobakterien, nicht aber von anderen Lebewesen produziert. Sie kommt zusammen mit Fructose natürlich in vielen Pflanzen vor, die in der menschlichen Ernährung verzehrt werden. Sie ist das Hauptkohlenhydrat vieler Früchte wie Ananas und Aprikosen; andere Früchte wie Birnen und Weintrauben haben Fruktose als Hauptkohlenhydrat. - Die vollständige Synthese von Saccharose gelang dem kanadischen Chemiker Raymond Lemieux im Jahr 1953. - Physikalische Eigenschaften - Saccharose karamellisiert bei 160 °C. - Saccharose ist in Wasser sehr gut lösich. Die Löslichkeit von Saccharose in nicht-wässrigen Lösungsmitteln ist in der Regel geringer. Darüber hinaus ist Saccharose in unpolaren Lösungsmitteln nicht löslich. Hohe Werte werden mit kondensiertem Ammoniak (72 %), Dimethylsulfoxid (42 %) und Methylamin (> 25 %) erzielt. Niedrigere Werte erhält man mit flüssigem Schwefeldioxid, Ameisen- und Essigsäure, Dimethylformamid, Pyridin (6 %), Propylenglykol, Glycerin (7 %), Methanol, Ethanol, Aceton und Dioxan. - Der Zuckergehalt wird durch den Brix-Grad angegeben (der dem Massenprozentsatz bei 20 °C entspricht). Die Konzentration einer wässrigen Lösung kann durch Messung der Dichte mit einem Mustimeter oder des Brechungsindex mit einem Refraktometer ermittelt werden. - Süßende Eigenschaften - Die Süßkraft von Saccharose dient als Referenzwert in der Süßstoffskala, d. h. sie wird konventionell als 1 angenommen. Die durchschnittliche Erkennungsgrenze von Saccharose liegt bei 0,017 mol l-1 (5,82 g/Liter). - Quellen für Saccharose - In der Natur kommt Saccharose in einer Vielzahl von Pflanzen vor, insbesondere in deren Wurzeln, Früchten und Nektar, wo sie zur Speicherung von Energie aus der Photosynthese dient. Viele Säugetiere, Vögel, Insekten und Bakterien ernähren sich von der Saccharose in den Pflanzen, manche sogar als Hauptnahrung. Bienen spielen in dieser Hinsicht eine besondere Rolle für die menschliche Ernährung, da sie aus dem Nektar Honig herstellen, der in allen Teilen der Welt verzehrt wird. Die Zuckerarten im Honig sind jedoch ganz überwiegend Glukose und Fruktose, mit nur Spuren von Saccharose. Während der Reifung der Früchte steigt der Saccharosegehalt in der Regel sehr schnell an, aber es gibt auch Früchte, die fast keine Saccharose enthalten. Beispiele hierfür sind Weintrauben, Kirschen, Heidelbeeren, Brombeeren, Feigen, Granatäpfel, Tomaten, Avocados, Zitronen und Limetten. - Verwendung in der Lebensmittelindustrie - Zucker als wichtige Lebensmittelzutat - Saccharose ist eine der am häufigsten verwendeten Zutaten in der Lebensmittelindustrie. Sie bildet die Grundlage für bestimmte Branchen wie die Süßwaren-, Backwaren-, Marmeladen- und Getränkeindustrie. - In der Pharmaindustrie wird es als Hilfsstoff verwendet. - Physikalische Chemie - Saccharose ist sehr gut wasserlöslich, wobei die Löslichkeit mit der Temperatur zunimmt. Sie ist relativ stabil, kann jedoch fermentieren (eine im Allgemeinen unerwünschte Entwicklung, außer bei alkoholischen Getränken) oder in Glukose und Fruktose hydrolysieren (in der Sprache der Süßwarenhersteller: invertieren), wobei dieses Phänomen kontrollierbar ist. - Bei der Verwendung in der Getränkeindustrie kann Saccharose bei der Wärmebehandlung von selbst invertieren. Da Invertzucker außerdem löslicher ist als Saccharose, kann er in seiner Gegenwart als Wasserbinder fungieren und die Kristallisation von Saccharose verhindern. - Saccharose verringert die Wasseraktivität von Produkten, die viel Saccharose enthalten, und ermöglicht so deren Konservierung. - Sie kann aufgrund ihrer agglomerierenden Eigenschaften auch als Texturhilfsmittel verwendet werden. – Korngröße - Verschiedene Kristallgrößen je nach Bedarf der Industrie : Kristallzucker; Zuckercouleur; Puderzucker; Kornzucker. - Verwendung in der Fermentation - Saccharose ist eines der klassischsten Gärungssubstrate. Viele Mikroorganismen können sie fermentieren, darunter auch der hochentwickelte Saccharomyces cerevisiae. - Verwendung in der Landwirtschaft - Saccharose wird in der Landwirtschaft verwendet. Das Versprühen von sehr geringen Dosen löslicher Zucker im Obstbau hat eine insektenabwehrende Wirkung, indem es die Wahrnehmung der Pflanze durch Schädlinge verändert.
FAQs
Was ist Saccharose?
"D(+)-Saccharose oder gewöhnlicher Zucker ist ein Disaccharid, das aus Glucose und Fructose, zwei Einfachzuckern oder Monosacchariden, besteht. Die Bindung, die die beiden Monosaccharide verbindet, ist vom O-glykosidischen Typ. Diese Bindung ist dicarbonyl, da die beiden reduzierenden Kohlenstoffe der beiden Monosaccharide die alpha(1-2)-Bindung der alpha-D-Glucose und beta-D-Fructose bilden. Er ist gemeinhin als Zucker, Saccharose oder Saccharose oder unter den folgenden chemischen Bezeichnungen bekannt: beta-D-Fructofuranosyl-alpha-D-glucopyranosid (IUPAC-Bezeichnung), alpha-D-Glucopyranosyl-beta-D-fructofuranosid, α-D-Glucopyranosyl-(1→2)-β-D-fructofuranosid; β-D-Fructofuranosyl-(2→1)-α-D-glucopyranosid; β-(2S,3S,4S,4S,5R)-Fructofuranosyl-α-(1R,2R,3S,4S,5R)-Glucopyranosid; α-(1R,2R,3S,4S,5R)-Glucopyranosyl-β-(2S,3S,4S,5R)-Fructofuranosid; ((2R,3R,4S,5S,5S,6R)-2-[(2S,3S,4S,5R)-3,4-Dihydroxy-2,5-bis(hydroxymethyl)oxapent-2-yl]oxy-6-(hydroxymethyl)oxahexan-3,4,5-triol). Die Summenformel von D(+)-Sucrose lautet C12H22O11. Er wird hauptsächlich aus Zuckerrohr und Zuckerrüben gewonnen. Saccharose hat keinen reduzierenden Charakter, da sie keine freien anomeren Kohlenstoffatome enthält, die anomeren Kohlenstoffe sind miteinander verbunden (beide OH-Gruppen der Carbonylkohlenstoffe sind an der O-glykosidischen Bindung beteiligt), d. h. die glykosidische Bindung von Saccharose wird zwischen den reduzierenden Enden von Glucose und Fructose gebildet und nicht zwischen dem reduzierenden Ende des einen und dem nicht reduzierenden Ende des anderen. Da Saccharose nicht reduzierend wirkt, ist sie daher im Fehling-Test negativ. Saccharose ist optisch aktiv. Optische Aktivität ist die Eigenschaft eines Stoffes, die Ebene des polarisierten Lichts zu drehen. Saccharose dreht die Polarisationsebene im Uhrzeigersinn (im Uhrzeigersinn) und wird daher als rechtsdrehender oder rechtsdrehender (+) Zucker bezeichnet. Die Nomenklatur D-L bietet eine schnelle Abkürzung für Enantiomere. Diese Verbindungen weisen zwei stereoisomere Formen auf und werden mit den Buchstaben D- und L- vor dem Namen der Verbindung bezeichnet, sind jedoch nicht mit der Nomenklatur zu verwechseln, die sich auf die Einteilung der Enantiomere in rechtsdrehende (+) und linksdrehende (-) Formen bezieht, was sich auf die optische Aktivität bezieht. Saccharose ist nicht nur das natürliche Süßungsmittel schlechthin in der menschlichen Ernährung, sondern auch der von der pharmazeutischen Industrie am häufigsten verwendete Zucker für die Herstellung von Sirup, Kautabletten, Dragees, Tabletten usw. Sirupe enthalten einen hohen Anteil an Saccharose, nicht nur, um Süße und Viskosität zu erreichen, sondern auch, um ihre Stabilität gegenüber Mikroorganismen zu erhöhen, da sie kein Wasser enthalten. Die hohen Zuckerkonzentrationen bewirken, dass der hohe osmotische Druck des Sirups das Wachstum von Bakterien verhindert. Saccharose ist auch ein Hilfsstoff in Impfstoffen. Da Impfstoffe biologische Präparate sind, können sie nach ihrer Herstellung instabil sein. Diese Instabilität kann die Sicherheit und Wirksamkeit des biologischen Produkts beeinträchtigen; Impfstoffe können empfindlich auf Hitze, Licht oder Veränderungen in der Umgebung reagieren. Saccharose bewahrt die Wirksamkeit von Impfstoffen, indem sie verhindert, dass die Moleküle bei der Herstellung, Lagerung, Verteilung und schließlich bei der Verabreichung an Patienten ihre Form verlieren. In der Lebensmittelindustrie dienen Zucker im Allgemeinen als Süßungsmittel, Geschmacksverstärker, Antioxidationsmittel und Konservierungsstoffe. Zu den chemischen Reaktionen von Zuckern gehören die Maillard-Reaktion oder die Bildung von bräunenden Verbindungen und die Karamellisierung. Vor allem Saccharose wirkt aufgrund ihrer natürlichen Benetzungseigenschaften als Stabilisator. Es wird als multifunktionales Produkt verwendet, da es nicht nur Lebensmittel süßt, sondern auch dazu beiträgt, dass Lebensmittel, insbesondere Back- und Süßwaren, frisch bleiben und ihre Feuchtigkeit behalten; es fördert die Gärung in Brot und anderen hefehaltigen Produkten, verbessert den Geschmack und die Textur von Lebensmitteln im Allgemeinen und wird auch als Konservierungsmittel und Süßungsmittel in Säften, kohlensäurehaltigen Getränken, Softdrinks und alkoholischen Getränken verwendet. Wie bei jedem anderen gelösten Stoff verändert die Zugabe von Zucker zu einem Gemisch den Siede- und Gefrierpunkt des Gemischs. Bei der Herstellung von Speiseeis beispielsweise senken Zucker den Gefrierpunkt und verhindern so, dass sich das Wasser im Inneren des Eises in Eis verwandelt, so dass trotz der niedrigen Temperaturen eine geschmeidige Textur entsteht, die sich gut verarbeiten lässt. Bei der Herstellung von Süßigkeiten hingegen ist die Erhöhung des Siedepunkts entscheidend für die Textur des Endprodukts. Im Allgemeinen führen höhere Temperaturen (höhere Zuckerkonzentration) zu härteren und steiferen Karamellen, während niedrigere Temperaturen zu weicheren Karamellen führen. Die endgültige Textur eines Bonbons hängt von der Konzentration des Zuckers ab, die wiederum vom Siedepunkt abhängt. Warum hat Saccharose kein Reduktionsvermögen?
Saccharose hat keinen reduzierenden Charakter, weil sie keine freien anomeren Kohlenstoffatome enthält, die anomeren Kohlenstoffe sind miteinander verbunden (beide OH-Gruppen der Carbonylkohlenstoffe sind an der O-glykosidischen Bindung beteiligt), d. h. die glykosidische Bindung in Saccharose wird zwischen den reduzierenden Enden von Glucose und Fructose gebildet, nicht zwischen dem reduzierenden Ende des einen und dem nicht reduzierenden Ende des anderen. Da Saccharose keinen reduzierenden Charakter hat, ist sie beim Fehling-Test negativ. Reduzierender Charakter tritt bei einem Disaccharid auf, wenn bei einem der Monosaccharide, aus denen es besteht, der anomere (oder Carbonyl-)Kohlenstoff frei ist, d. h. wenn dieser Kohlenstoff nicht Teil der O-glycosidischen Bindung ist. Mit anderen Worten, wenn die O-glykosidische Bindung monocarbonyl ist, ist das resultierende Disaccharid reduzierend (Laktose, Maltose), während wenn die O-glykosidische Bindung dicarbonyl ist, das resultierende Disaccharid nicht reduzierend ist (Saccharose, Trehalose). Der Fehling-Test (entdeckt von dem deutschen Chemiker Hermann von Fehling) wird zum Nachweis von reduzierenden Substanzen, insbesondere von reduzierenden Zuckern, verwendet. Sie beruht auf der Reduktionskraft der Carbonylgruppe eines Aldehyds, der durch Reduktion von Kupfer(II)-Kupfersalz in einem alkalischen Medium zu Kupfer(I)-oxid sauer wird und einen roten Niederschlag bildet. Ein wichtiger Aspekt dieser Reaktion ist, dass die Aldehydform leicht nachgewiesen werden kann, auch wenn sie nur in sehr geringen Mengen vorliegt. Reduziert ein Zucker das Fehlingsche Reagenz zu rotem Kupfer(I)oxid, so spricht man von einem reduzierenden Zucker. Fehling (blau) + nicht-reduzierender Zucker = blaue Farbe - Fehling (blau) + reduzierender Zucker = ziegelrote Farbe Wozu dient der Fehling-Test?
Der Fehling-Test (entdeckt von dem deutschen Chemiker Hermann von Fehling) wird zum Nachweis von reduzierenden Substanzen, insbesondere reduzierenden Zuckern, verwendet. Sie beruht auf der Reduktionskraft der Carbonylgruppe eines Aldehyds, der sauer wird, indem er das Kupfer(II)-Kupfersalz in einem alkalischen Medium zu Kupfer(I)-oxid reduziert, das einen roten Niederschlag bildet. Ein wichtiger Aspekt dieser Reaktion ist, dass die Aldehydform leicht nachgewiesen werden kann, auch wenn sie nur in sehr geringen Mengen vorliegt. Reduziert ein Zucker das Fehlingsche Reagenz zu rotem Kupfer(I)oxid, so spricht man von einem reduzierenden Zucker. Fehling (blau) + nicht reduzierender Zucker = blaue Farbe; Fehling (blau) + reduzierender Zucker = ziegelrote Farbe Welche Anwendungen hat Saccharose?
Saccharose ist nicht nur das natürliche Süßungsmittel schlechthin in der menschlichen Ernährung, sondern auch der von der pharmazeutischen Industrie am häufigsten verwendete Zucker für die Herstellung von Sirup, Kautabletten, Dragees, Tabletten usw. Sirupe enthalten einen hohen Anteil an Saccharose, nicht nur, um Süße und Viskosität zu erreichen, sondern auch, um ihre Stabilität gegenüber Mikroorganismen zu erhöhen, da sie kein Wasser enthalten. Die hohen Zuckerkonzentrationen bewirken, dass der hohe osmotische Druck des Sirups das Wachstum von Bakterien verhindert. Saccharose ist auch ein Hilfsstoff in Impfstoffen. Da Impfstoffe biologische Präparate sind, können sie nach ihrer Herstellung instabil sein. Diese Instabilität kann die Sicherheit und Wirksamkeit des biologischen Produkts beeinträchtigen; Impfstoffe können empfindlich auf Hitze, Licht oder Veränderungen in der Umgebung reagieren. Saccharose bewahrt die Wirksamkeit von Impfstoffen, indem sie verhindert, dass die Moleküle bei der Herstellung, Lagerung, Verteilung und schließlich bei der Verabreichung an Patienten ihre Form verlieren. In der Lebensmittelindustrie dienen Zucker im Allgemeinen als Süßungsmittel, Geschmacksverstärker, Antioxidationsmittel und Konservierungsstoffe. Zu den chemischen Reaktionen von Zuckern gehören die Maillard-Reaktion oder die Bildung von bräunenden Verbindungen und die Karamellisierung. Insbesondere Saccharose wirkt aufgrund ihrer natürlichen Benetzungseigenschaften als Stabilisator und wird als multifunktionales Produkt verwendet, da sie nicht nur Lebensmittel süßt, sondern auch dazu beiträgt, dass Lebensmittel, insbesondere Back- und Süßwaren, frisch bleiben und ihre Feuchtigkeit behalten; sie fördert die Gärung in Brot und anderen hefehaltigen Produkten, verbessert den Geschmack und die Textur von Lebensmitteln im Allgemeinen und dient auch als Konservierungsmittel und Süßungsmittel in Säften, kohlensäurehaltigen Getränken, Softdrinks und alkoholischen Getränken. Wie bei jedem anderen gelösten Stoff verändert die Zugabe von Zucker zu einem Gemisch dessen Siede- und Gefrierpunkt. Bei der Herstellung von Speiseeis beispielsweise senken Zucker den Gefrierpunkt und verhindern so, dass das im Eis enthaltene Wasser zu Eis wird. Bei der Herstellung von Süßigkeiten hingegen ist die Erhöhung des Siedepunkts ausschlaggebend für die Textur des Endprodukts. Im Allgemeinen führen höhere Temperaturen (höhere Zuckerkonzentration) zu härteren und steiferen Karamellen, während niedrigere Temperaturen zu weicheren Karamellen führen. Die endgültige Textur eines Bonbons hängt von der Zuckerkonzentration ab, die wiederum vom Siedepunkt abhängt. Wozu wird D(+)-Zucker verwendet?
D(+)-Zucker, oder einfach Saccharose, ist der übliche Zucker. D(+)-Sucrose ist nicht nur das natürliche Süßungsmittel schlechthin in der menschlichen Ernährung, sondern auch der Zucker, der von der pharmazeutischen Industrie am häufigsten für die Herstellung von Sirup, Kautabletten, Dragees, Tabletten usw. verwendet wird. Sirupe enthalten einen hohen Anteil an Saccharose, nicht nur, um Süße und Viskosität zu erreichen, sondern auch, um ihre Stabilität gegenüber Mikroorganismen zu erhöhen, da sie kein Wasser enthalten. Die hohen Zuckerkonzentrationen bewirken, dass der hohe osmotische Druck des Sirups das Wachstum von Bakterien verhindert. Saccharose ist auch ein Hilfsstoff in Impfstoffen. Da Impfstoffe biologische Präparate sind, können sie nach ihrer Herstellung instabil sein. Diese Instabilität kann die Sicherheit und Wirksamkeit des biologischen Produkts beeinträchtigen; Impfstoffe können empfindlich auf Hitze, Licht oder Veränderungen in der Umgebung reagieren. Saccharose bewahrt die Wirksamkeit von Impfstoffen, indem sie verhindert, dass die Moleküle bei der Herstellung, Lagerung, Verteilung und schließlich bei der Verabreichung an Patienten ihre Form verlieren. In der Lebensmittelindustrie dienen Zucker im Allgemeinen als Süßungsmittel, Geschmacksverstärker, Antioxidationsmittel und Konservierungsstoffe. Zu den chemischen Reaktionen von Zuckern gehören die Maillard-Reaktion oder die Bildung von bräunenden Verbindungen und die Karamellisierung. Insbesondere Saccharose wirkt aufgrund ihrer natürlichen Benetzungseigenschaften als Stabilisator und wird als multifunktionales Produkt verwendet, da sie nicht nur Lebensmittel süßt, sondern auch dazu beiträgt, dass Lebensmittel, insbesondere Back- und Süßwaren, frisch bleiben und ihre Feuchtigkeit behalten; sie fördert die Gärung in Brot und anderen hefehaltigen Produkten, verbessert den Geschmack und die Textur von Lebensmitteln im Allgemeinen und dient auch als Konservierungsmittel und Süßungsmittel in Säften, kohlensäurehaltigen Getränken, Softdrinks und alkoholischen Getränken. Wie bei jedem anderen gelösten Stoff ändert sich durch die Zugabe von Zucker zu einem Gemisch der Siede- und Gefrierpunkt des Gemischs. Bei der Herstellung von Speiseeis beispielsweise senken Zucker den Gefrierpunkt und verhindern so, dass sich das Wasser im Inneren des Eises in Eis verwandelt, so dass trotz der niedrigen Temperaturen eine geschmeidige Textur entsteht, die sich gut verarbeiten lässt. Bei der Herstellung von Süßigkeiten hingegen ist die Erhöhung des Siedepunkts entscheidend für die Textur des Endprodukts. Im Allgemeinen führen höhere Temperaturen (höhere Zuckerkonzentration) zu härteren und steiferen Karamellen, während niedrigere Temperaturen zu weicheren Karamellen führen. Die endgültige Textur eines Bonbons hängt von der Zuckerkonzentration ab, die wiederum vom Siedepunkt abhängt. Was ist die Rolle von Saccharose als Hilfsstoff?
Sucrose kann in der pharmazeutischen Industrie mehrere Funktionen erfüllen: Sie kann als Füllstoff oder Verdünnungsmittel dienen, wenn beispielsweise die Wirkstoffmenge zu gering ist, um bequem gehandhabt werden zu können; als Bindemittel, um die Bestandteile einer Formulierung zusammenzuhalten, beispielsweise in einer Tablette; als Überzugsmaterial, um die Viskosität zu erhöhen oder auch als eine der Hauptfunktionen von Saccharose: Geschmack, um unangenehme Geschmäcker von Wirkstoffen zu überdecken und pharmazeutische Produkte schmackhafter zu machen. Die hohen Zuckerkonzentrationen in Sirupen bedeuten, dass der hohe osmotische Druck des Sirups das Bakterienwachstum verhindert. Saccharose ist auch ein Hilfsstoff in Impfstoffen. Saccharose bewahrt die Wirksamkeit von Impfstoffen, indem sie verhindert, dass die Moleküle bei der Herstellung, Lagerung, Verteilung und schließlich bei der Verabreichung an Patienten ihre Form verlieren. Warum wird Saccharose D(+)-Saccharose genannt?
Saccharose ist optisch aktiv. Optische Aktivität ist die Eigenschaft eines Stoffes, die Ebene des polarisierten Lichts zu drehen. Da Saccharose die Polarisationsebene im Uhrzeigersinn dreht, wird sie als rechtsdrehend oder rechtsdrehender Zucker bezeichnet; sie ist ein optisches (+) Isomer. Die Nomenklatur D-L bietet eine schnelle Abkürzung für Enantiomere. Diese Verbindungen weisen zwei stereoisomere Formen auf und werden mit den Buchstaben D- und L- vor dem Namen der Verbindung bezeichnet, sind jedoch nicht mit der Nomenklatur zu verwechseln, die sich auf die Einteilung der Enantiomere in rechtsdrehende (+) und linksdrehende (-) Formen bezieht, die sich auf die optische Aktivität beziehen. Die Symbole R und S werden derzeit verwendet, um die Konfiguration, d. h. die Anordnung der Atome oder Atomgruppen im Raum, anzugeben; in einigen Fällen können auch andere Begriffe wie D und L verwendet werden. Was bedeutet es, dass ein Zucker reduzierend ist?
Ein reduzierender Zucker ist jeder Zucker, der als Reduktionsmittel wirken kann. In alkalischer Lösung kann ein reduzierender Zucker einen Aldehyd oder ein Keton bilden, wodurch er als Reduktionsmittel fungieren kann, z. B. in Benedict's Reagenz. Bei einer solchen Reaktion wird der Zucker in eine Carbonsäure umgewandelt. Alle Monosaccharide sind reduzierende Zucker, ebenso wie einige Disaccharide, einige Oligosaccharide und einige Polysaccharide. Monosaccharide lassen sich in zwei Gruppen einteilen: Aldosen, die eine Aldehydgruppe haben, und Ketosen, die eine Ketongruppe haben. Ketosen müssen zunächst zu Aldosen tautomerisieren, bevor sie als reduzierende Zucker wirken können. Die in der Ernährung häufig vorkommenden Monosaccharide Galaktose, Glukose und Fruktose sind allesamt reduzierende Zucker. Disaccharide werden aus zwei Monosacchariden gebildet und können entweder als reduzierend oder nicht-reduzierend klassifiziert werden. Nicht reduzierende Disaccharide wie Saccharose und Trehalose haben glykosidische Bindungen zwischen ihren anomeren Kohlenstoffen und können daher nicht in eine offenkettige Form mit einer Aldehydgruppe umgewandelt werden; sie sind zyklisch geschlossen. Bei reduzierenden Disacchariden wie Laktose und Maltose ist nur einer der beiden anomeren Kohlenstoffe an der glykosidischen Bindung beteiligt, während der andere frei ist und in eine offenkettige Form mit einer Aldehydgruppe umgewandelt werden kann. Die funktionelle Aldehydgruppe ermöglicht es dem Zucker, als Reduktionsmittel zu wirken, z. B. im Tollens-Test oder Benedict-Test. Die zyklischen Hemiacetalformen von Aldosen können geöffnet werden, um einen Aldehyd freizusetzen, und bestimmte Ketosen können durch Tautomerisierung zu Aldosen werden. Acetale, auch solche, die in Polysaccharidbindungen vorkommen, lassen sich jedoch nicht ohne weiteres in freie Aldehyde umwandeln. Reduzierende Zucker reagieren mit Aminosäuren in der Maillard-Reaktion, einer Reihe von Reaktionen, die auftreten, wenn Lebensmittel bei hohen Temperaturen gegart werden, und die für den Geschmack von Lebensmitteln wichtig sind. Darüber hinaus ist der Gehalt an reduzierenden Zuckern in Wein, Saft und Rohrzucker ein Indikator für die Qualität dieser Lebensmittel. Was ist der Schmelzpunkt von Saccharose?
Keine. Saccharose zersetzt sich bei 186 °C. Sie schmilzt nicht, aber wenn sie die Zersetzungstemperatur erreicht, zerfällt Saccharose in Fruktose und Glukose. Das Erhitzen von Saccharose ist ein komplexer thermischer Prozess, der sowohl Schmelzen als auch Zersetzung beinhaltet. Je nach Erhitzungsgeschwindigkeit werden unterschiedliche Dinge beobachtet. Grundsätzlich beginnt sich die Saccharose zu zersetzen, wenn sie zu schmelzen beginnt. Wenn während des Erhitzens Wasser vorhanden ist, kommt es zu einer Reaktion, die als Saccharose-Inversion bekannt ist, und die Saccharose zerfällt in ihre Bestandteile, ein Glukosemolekül und ein Fruktosemolekül. Wenn jedoch trockene Saccharose bis zu ihrem Schmelz- oder Zersetzungspunkt erhitzt wird, geschehen komplexere Dinge. Zunächst werden erhebliche Mengen an Glukose nachgewiesen. Fortgesetztes Erhitzen führt zur "Karamellisierung". Die Karamellisierung ist ein Kondensationsprozess, bei dem der Saccharose Wasser entzogen wird; auf den anfänglichen Wasserverlust folgen Isomerisierung und Polymerisation. Man geht davon aus, dass sich bei der Karamellisierung mehrere tausend verschiedene Verbindungen bilden. Derzeit laufen noch Studien, um sie alle zu identifizieren. Wenn diese komplexe Mischung abkühlt, handelt es sich nicht mehr um Saccharose. Wie groß ist die Löslichkeit von Saccharose?
Die Löslichkeit von Saccharose in Wasser beträgt 2039 g/L bei 20 °C. Was versteht man unter Invertzucker?
Invertzucker ist ein Sirup, der aus Glucose und Fructose (Monosaccharide) besteht und durch Hydrolyse von Saccharose (Disaccharid) gewonnen wird. Bei der Hydrolyse von Saccharose entsteht ein äquimolares Gemisch aus Fruktose und Glukose, das im Handel als Invertzucker bekannt ist und so genannt wird, weil sich seine optischen Eigenschaften durch die Rotation von einer positiven oder rechtsdrehenden Rotation zu einer negativen oder linksdrehenden Rotation ändern. Saccharose ist rechtsdrehend, mit einer spezifischen Drehung von +66,5°; Bei der Spaltung in rechtsdrehende Glucose (oder Dextrose) mit einer spezifischen Drehung von [α] D = +52,7° und in stark linksdrehende Fructose (Lävulose) mit einer spezifischen Drehung von [α] D = -92° ist das entstehende Gemisch linksdrehend, d. h. die Drehrichtung der Schwingungsebene des Lichts hat sich gegenüber der ursprünglichen Saccharose umgekehrt, daher die Bezeichnung Invertzucker. Die Inversion von Saccharose kann durch saure Hydrolyse oder enzymatische Hydrolyse (mit Invertase) erreicht werden. Invertzucker kann auch als Invertzuckersirup, Invertzuckersirup, einfacher Sirup, Zuckersirup, USP-Sirup, Invertzucker, Zuckerwasser oder Barsirup bezeichnet werden. Invertzuckersirup ist 30 % süßer als Saccharose und kann leichter in Lebensmittel und pharmazeutische Zubereitungen eingearbeitet werden, da er nicht die Kristallisationsprobleme seines Vorläufers (Saccharose) aufweist, der in hochkonzentrierten Lösungen kristallisiert. Was ist die spezifische Drehung von D(+)-Sucrose?
Die spezifische Drehung von D-(+)-Sucrose α 20/D c=26 (in H2O) beträgt +66,5°. Im Allgemeinen nimmt die Drehung mit steigender Temperatur linear ab; der Unterschied zwischen der bei 20 und 25 °C beobachteten Drehung ist jedoch im Allgemeinen vernachlässigbar. In den Arzneibüchern werden die Messungen üblicherweise bei 25 °C unter Verwendung der Natrium-D-Linie bei einer Wellenlänge von 589 nm durchgeführt. Die so ermittelte spezifische Drehung wird als α 25/D ausgedrückt. Wie wird die spezifische Drehung von Saccharose gemessen?
Die spezifische Drehung ([α]) ist eine Eigenschaft einer chiralen chemischen Verbindung. Sie ist definiert als die Änderung der Ausrichtung von in der Ebene polarisiertem monochromatischem Licht pro Einheitsabstandskonzentrationsprodukt, wenn Licht durch eine Probe einer Verbindung in Lösung fällt. Verbindungen, die die Polarisationsebene eines planpolarisierten Lichtstrahls im Uhrzeigersinn drehen, werden als rechtsdrehend bezeichnet, was positiven Werten der spezifischen Drehung entspricht, während Verbindungen, die die Polarisationsebene von planpolarisiertem Licht gegen den Uhrzeigersinn drehen, als linksdrehend bezeichnet werden, was negativen Werten entspricht. Wenn eine Verbindung in der Lage ist, die Polarisationsebene von planar polarisiertem Licht zu drehen, wird sie als "optisch aktiv" bezeichnet. Die Polarimetrie ist ein Verfahren zur Unterscheidung optisch aktiver Isomere durch Messung der optischen Drehung einer Substanz; sie ist auch ein wichtiges Kriterium für Identität und Reinheit und kann für quantitative Zwecke verwendet werden. Wie lautet die CAS-Nummer von Saccharose?
Die CAS-Nummer von Saccharose ist 57-50-1. Was ist die CAS-Nummer 57-50-1?
Die CAS-Nummer 57-50-1 steht für D(+)-Saccharose. Er ist gemeinhin als Zucker, Saccharose oder Saccharose oder unter den folgenden chemischen Bezeichnungen bekannt: beta-D-Fructofuranosyl-alpha-D-glucopyranosid (IUPAC-Name), alpha-D-Glucopyranosyl-beta-D-fructofuranosid, α-D-Glucopyranosyl-(1→2)-β-D-fructofuranosid; β-D-Fructofuranosyl-(2→1)-α-D-glucopyranosid; β-(2S,3S,4S,5R)-Fructofuranosyl-α-(1R,2R,3S,4S,5R)-glucopyranosid; α-(1R,2R,3S,3S,4S,5R)-Glucopyranosyl-β-(2S,3S,4S,5R)-fructofuranosid; ((2R,3R,4S,5S,5S,6R)-2-[(2S,3S,4S,5R)-3,4-Dihydroxy-2,5-bis(hydroxymethyl)oxapent-2-yl]oxy-6-(hydroxymethyl)oxahexan-3,4,5-triol) Was sind Brixgrade?
Die Brixmessung ist eine bekannte Anwendung unter anderem in der Lebensmittel- und Getränkeindustrie. Streng genommen ist die Brix-Messung die Bestimmung des Gehalts an reiner Saccharose in Wasser: 1 Grad Brix (°Bx) = 1 g Saccharose / in 100 g Lösung Bei Obst und Gemüse gibt dieser Wert die Menge des vorhandenen Zuckers (Saccharose) an, der den Geschmack entscheidend beeinflusst. Die Messung des Zuckergehalts in frischem Obst ist unerlässlich, um den Reifegrad und den optimalen Erntezeitpunkt zu bestimmen, der von der Art des Produkts und der jeweiligen Sorte abhängt. Es gibt nationale und internationale Qualitätsvorschriften, die Mindestbrixwerte für die angemessene Vermarktung jedes Produkts festlegen". Wie wird der Brix-Grad gemessen?
Zur Messung des Brix-Grads können verschiedene Geräte verwendet werden, das gebräuchlichste ist jedoch das Refraktometer. Ein Refraktometer bestimmt den Brix-Wert durch Messung der Brechung des Lichts, das durch eine Flüssigkeitsprobe fällt. Flüssigkeiten, die Zucker und/oder andere gelöste Feststoffe enthalten, sind dichter als Wasser und verursachen eine stärkere Lichtbrechung beim Durchgang des Lichts. Das Gerät vergleicht dies mit der Lichtbrechung durch Wasser und gibt einen Brixwert an. Der Brechungsindex hängt nicht nur von der Wellenlänge ab, die zur Messung verwendet wird, sondern auch von der Temperatur der gemessenen Lösung. Es besteht ein direkter Zusammenhang zwischen dem Brechungsindex und dem Brix-Wert. Der gemessene Brechungsindex wird direkt in den Feststoffgehalt nach Gewicht (°Brix) umgerechnet. Die Brix-Skala ist eine gängige Skala, die vom Brechungsindex einer Lösung bei 20 °C abgeleitet ist. Wo kann man Saccharose kaufen
Sie können Saccharose von ITW Reagents über sein weltweites Händlernetz oder über den Online-Shop kaufen, wenn Sie ein registrierter Kunde von ITW Reagents sind. Wenn Sie Saccharose für Produktionsprozesse kaufen möchten, wenden Sie sich bitte an unsere Vertriebshändler. Folgen Sie diesem Link, um einen Händler in Ihrem Land zu finden https://itwreagents.com/rest-of-world/es/distribuidores-rw.