Presentaciones (1)
| código | presentación | precio por unidad | precio de caja por unidad | |
|---|---|---|---|---|
| Código y embalaje | Precio por unidad | |||

|
código
A1052,1000
|
presentación
1 kg
|
Producto disponible hasta agotar existencias.
|
|
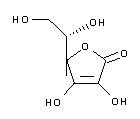
Datos técnicos
- Descripción Física:
- Sólido
- Código de Producto:
- A1052
- Nombre de Producto:
- Ácido L(+)-Ascórbico polvo BioChemica
- Especificaciones:
- Riqueza (titr.): min. 99 %
α20°C/D; 10 %, H2O: +20,5° - +21,5°
pH (5 %; H2O; 20°C): 2,2 - 2,5
Metales pesados (en Pb): max. 0,0005 %
Insolubles: Conforme ensayo
Ácido oxálico: max. 0,3 %
Cloruro: max. 0,005 %
Sulfato: max. 0,002 %
- WGK:
- 1
- Almacenaje:
- Temperatura ambiente
- EINECS:
- 200-066-2
- NC:
- 29362700





